Etiquetas
cuantización, Einstein, modelo atómico, Niels Bohr, Nobel Prize, onda partícula, química cuántica, tabla periódica

El cráter lunar Bohr lleva este nombre en su memoria. El elemento químico bohrio se denominó así en su honor, al igual que el asteroide (3948) Bohr descubierto por Poul Jensen.
El “modelo cuántico de Bohr”, fue un enorme avance en la época, porqué demostró que la cuántica podía explicar fenómenos importantes como la composición de la materia en su nivel elemental y la reactividad química. Posteriormente este modelo permitió dar una explicación a los espectros de emisión de rayos X, a la absorción – emisión de luz por los átomos y a la variación de las propiedades químicas de los elementos.
La mecánica clásica, newtoniana, presentaba una descripción objetiva de la realidad, una separación entre objeto y sujeto, en la cuántica la separación se produce de una manera arbitraria, con la introducción del “cuanto de acción” de Planck en los procesos atómicos, se pone en cuestión la concepción determinista de la naturaleza.
El nombre de Bohr va unido a la interpretación de Copenhague, se entiende la interpretación de la mecánica cuántica en la que un sistema puede describirse mediante una “función de onda”. Una posición definida o “espín de la partícula” no se produce hasta que es observada.
Niels Bohr, nace en 1885 en Copenhague, realizó un curso de filosofía en 1903 con el profesor Harald Hoffding, estudió física con Christian Christiansen, se licenció en 1909; tras doctorarse en la Universidad de Copenhague en 1911 pasó un año en Inglaterra de postdoctorado en Cambridge y Manchester teniendo como maestro a Ernest Rutherford. En 1916, Niels Bohr comenzó a ejercer como profesor de física teórica en la Universidad de Copenhague, consiguiendo los fondos para crear el “Instituto Nórdico de Física Teórica”, que dirigió desde 1920 hasta su fallecimiento. En 1943, con la Segunda Guerra Mundial, Bohr escapó a Suecia, viajando posteriormente a Londres. Una vez a salvo, trabajó para el Proyecto Manhattan de los Álamos, Nuevo México (EE.UU.). Después de la guerra, retornó a Copenhague, donde residió hasta su fallecimiento en 1962.
A través de Hoffding, llegó a la filosofía existencialista de Kierkegaard. Filosofía de continuidad en el tiempo en que la discontinuidad se había convertido en una realidad Max Planck, descubrió el “cuanto de acción” en 1900. Hoffding creía que se daban “saltos” en la naturaleza inanimada, así Bohr renunció a las explicaciones causales y defendió cambios espontáneos antes de familiarizarse con el existencialismo de Kierkegaard. A lo largo de la carrera de Bohr se reconcilia la teoría clásica y la teoría cuántica en algo racional.
En la física clásica existe una continuidad hay coordenadas de:
• Espacio
• Tiempo
• Energía
• Momento
En la física cuántica se aceptan como intrínsecas nociones de:
• Indeterminación
• Descripción estadística
• Distribución probabilista
Sus trabajos adquieren una doble importancia en la historia de la física del siglo XX:
a) Primer esbozo de una teoría coherente sobre la constitución del átomo.
b) Se convertía en un avance decisivo de la concepción cuántica al establecer un grado de generalidad.
“El modelo atómico de Bohr” se basa en tres postulados:
1. Los electrones describen órbitas circulares en torno al núcleo del átomo sin radiar energía.
2. No todas las órbitas para el electrón están permitidas, solo se pueden encontrar órbitas cuyo radio cumpla que el “momento angular”, L, del electrón sea un múltiplo entero.
3. El electrón solo emite o absorbe energía en los saltos de una órbita permitida a otra. En dicho cambio emite o absorbe un fotón cuya energía es la diferencia entre ambos niveles.
El primer modelo atómico de Bohr, se presentó en 1913, en “On the constitution of atoms and molecules”, aportaba la base teórica para el modelo atómico construido por Rutherford en 1911. Resolvía la constitución del átomo a través de los conceptos cuánticos: los electrones orbitan alrededor de un núcleo central y alcanzan estabilidad: cuantificación del momento angular. El tránsito de los electrones de una órbita a otra viene acompañado de la absorción o emisión de energía en forma de luz, explicando el espectro de emisión del hidrógeno:
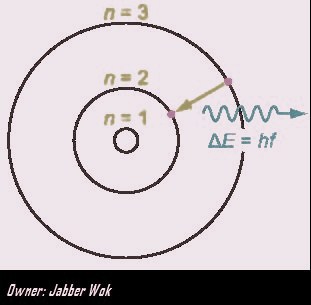
Un solo electrón de masa “m” viajaba en órbita circular de radio “r”, a una velocidad “v”, en torno a un núcleo dotado de carga positiva. El “momento angular” del electrón sería entonces mxvxr, Bohr propuso que los electrones pudieran ocupar solo órbitas en las que este momento angular presentara ciertos valores fijos: h/2pi, 2h/2pi/, 3h/3pi…h/npi donde “h” es la constante de Planck. Se cuantifica el momento algunar, presenta solo determinados valores, cada uno de los cuales es múltiplo de h/2pi. Bohr suponía que, cuando el átomo emitía o absorbía radiación de frecuencia, el electrón saltaba de una órbita a la siguiente; la energía emitida o absorbida en cada salto era igual a hxv.
Bohr estableció la alianza entre la física clásica y la cuántica, con sus dos principios:
• “Principio de correspondencia” en la obra “On the quantum theory o line-spectra. Part I”, publicado en 1918.
• “Principio de complementariedad” en la obra “Atomic theory and the description o nature”, propone la complementariedad de las representaciones de los sucesos, la teoría cuántica es una generalización racional de la mecánica clásica.
En 1922 Bohr actualizó las tablas periódicas de los elementos propuestas por Bayley y Thomsen en las que se había iniciado una separación entre los grupos principales y secundarios, Bohr alargó el sistema de Thomsen introduciendo un grupo de elementos (periodo 7º) que comenzaba con el Ac como homólogo del La y donde se iniciaba el llenado del orbital 5f. Dejó también 14 espacios para colocar las tierras raras que comenzaban después del U.
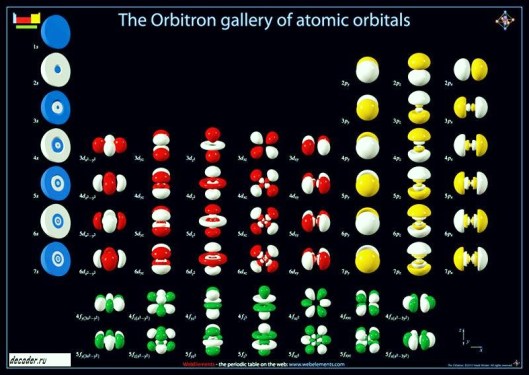
Propuso un modelo atómico según el cual los electrones se agrupan alrededor del núcleo formando capas concéntricas de modo que cumplen unas condiciones determinadas. Aquellos elementos que pertenecen a un mismo grupo habrían de tener una configuración electrónica similar. Los átomos no son indivisibles sino que están formados por partículas subatómicas con cargas eléctricas y masas características, los átomos tenían concentraciones de masa y espacios vacíos, así Rutherford y Bohr, propusieron los “modelos planetarios” o “nucleares para los átomos”.
Los átomos tienen una parte central llamada “núcleo” en la que reside la casi totalidad de la masa del átomo, el núcleo está cargado positivamente: los protones están en el núcleo del átomo. Los electrones giran alrededor del núcleo. Cada capa tiene una energía distinta, a las capas de Bohr se les llama también “niveles de energía”. Los electrones no pueden tomar cualquier valor de energía se les conoce como “cuantización de la energía”: “el modelo atómico de Bohr” es por tanto un modelo “cuántico”. El estado de menor energía de un átomo sería aquel en el que el valor de las energías de los electrones sumadas nos diera el valor más negativo.
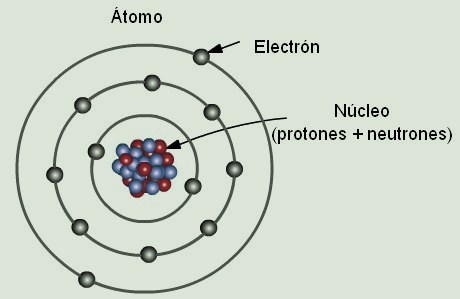
Las capas de Bohr se denominan alfabéticamente a partir de la letra K y, de acuerdo con la teoría, no pueden contener cualquier número de electrones:
• CAPA K: 2 electrones
• CAPA L: 8 electrones
• CAPA M: 18 electrones
• CAPA N: 32 electrones
Los átomos son eléctricamente neutros, el número de protones debe ser igual al número de electrones, la distribución electrónica para algunos átomos de acuerdo con el modelo de Bohr nos genera la forma más usada y más conocida de la tabla periódica, la llamada “Tabla periódica Larga” o “Tabla de Bohr” o “Tabla de Bohr y Sommerfeld”.
En 1922 recibió el Premio Nobel de Física por sus trabajos sobre la estructura atómica y la radiación. Concluye que la luz presentaba una dualidad “onda-partícula” mostrando propiedades mutuamente excluyentes según el caso. Su hijo Aage Niels Bohr, obtuvo también el premio Nobel de Física en 1975.
En 1933 Bohr propuso la hipótesis de la “gota liquida”, teoría que permitía explicar las desintegraciones nucleares (entre ellas la fisión del isótopo uranio 235).
Los nuevos conceptos “cuánticos” defendidos por Bohr no eran compartidos por el racionalismo de Einstein, era reacio a interpretaciones de física filosóficas, de donde surgía la nueva mecánica, la materia ordenada surgía del desorden regido por el azar, el comportamiento de la materia depende del hecho de observarla y el concepto del cuanto:
“Dios no juega a los dados con el Universo”, “la Luna aún sigue ahí, aunque no la mire”, “esta espeluznante acción a distancia”.
Einstein decía que el universo material era “local y real”, donde lo local indicaba que nada puede superar la velocidad de la luz. Bohr aludía a la “función de onda” de las partículas subatómicas y al estado de “superposición” que pueden presentar estas. Esto podía ser producto de una de dos alternativas: a) las partículas subatómicas en dos puntos alejados del universo se envían información sobre sus estados a velocidades superiores a la de la luz con lo cual la superposición se explicaría por la presencia de más de un electrón que se comunican en distintos puntos del universo o b) las partículas subatómicas pueden existir en dos o más estados a la vez.
Uno de los más famosos estudiantes de Bohr fue Werner Heisenberg, el líder del proyecto alemán de bomba atómica.
Bohr después de la guerra, se convirtió en un defensor el desarme nuclear. Fue el primero en recibir, en 1958, el premio Átomos para la Paz.
Tiene varios libros interesantes: “Teoría de los espectros y constitución atómica”, “El mecanismo de la fisión nuclear”, “Física atómica y conocimiento humano”.
Bibliografía:
• NobelPrize.org Niels Bohr
https://www.nobelprize.org/nobel_prizes/physics/laureates/1922/
• Roberto Angeloni, Leo S. Olschki, “Unity and continuity in Niels Bohr´s philosophy of physics”, Bibliotea di Nuncius, Florencia, 2013.
• Leidys Laura Pérez González, Noel David Pérez Acosta, “El modelo atómico de Bohr y el desarrollo de la nanociencia en el cuidado de la salud”, Universidad Central “Marta Abreu” de las Villas, Santa Clara, Villa Clara, Cuba; Policlínico “Idalberto Revuelta”, Sagua la Grande, Villa Clara. 2016.
• Wikipedia
Links relacionados:
• Universidad Rice, Relativistic Heavy Ion Physics Group Prof. Wei Li
http://wl33.web.rice.edu/index.html
• Universidad Rice; Who knew excited atoms can make like Mars?
http://explore.rice.edu/WhoKnew_Template.aspx?id=5439
• Universidad Rice: Physicists create millimeter-sized ‘Bohr atom’
http://news.rice.edu/2008/06/26/physicists-create-millimeter-sized-bohr-atom/
• Universidad de Copenhague, Instituto Niels Bohr
http://www.nbi.ku.dk/english/
