Durante los siglos XIV que se desarrolló la epidemia de peste, no se entendía el mecanismo de difusión, hasta observar Pasteur la transmisión por “microorganismos” surgiendo la “asepsia” a partir del siglo XIX. La “teoría microbiana” supuso un paso fundamental en la medicina moderna y la microbiología clínica (virus, bacterias, parásitos y hongos), con grandes avances en el desarrollo de la medicina: los antibióticos, las vacunas, la esterilización y la higiene.
Fue durante el renacimiento cuando la gente se cubría la cara para evitar contagiarse utilizaban pañuelos en la nariz y los médicos “máscara con forma de pico”, en 1890 el microbiólogo alemán Carl Flügge, demostró que había gotas diminutas que se transmitían al hablar, toser o estornudar, posteriormente Mikulicz un cirujano rumano apoya el uso del cubrebocas, y Paul Berger en 1897 en París lo usa por primera vez en una operación, siendo obligatorias en 1926 al descubrir microorganismos de la nariz y la boca de cirujanos y enfermeras en la heridas infectadas de los pacientes.

Ya durante el siglo XIV con la pandemia de la “peste negra” afectando a Europa, África y Asia hay un intento de aislarse del paciente, evitando el contacto del “aire podrido” mediante una máscara en forma de “pico de cuervo” como medida de higiene.
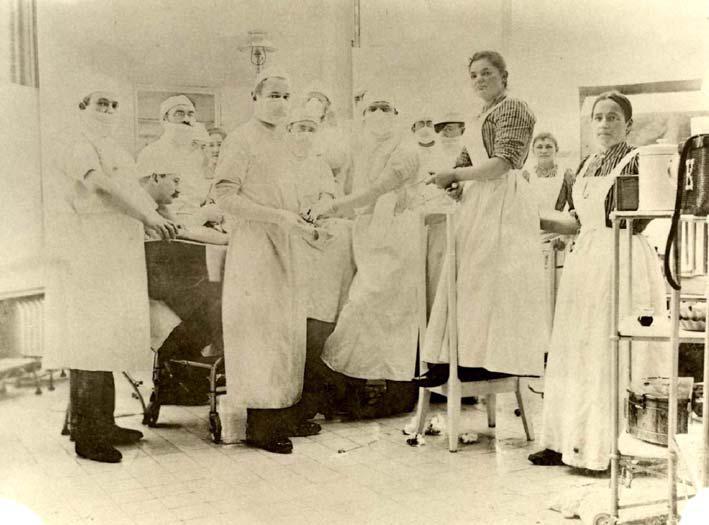
Las técnicas de asepsia: mantenimiento de las condiciones estériles para no causar infecciones en los procedimientos quirúrgicos se desarrollan en el siglo XIX. Con el descubrimiento de los anestésicos las operaciones se hacen más largas con más posibilidades de infección. El uso de la máscara, los guantes y los trajes de quirófano se hicieron más usuales.
La teoría de la asepsia es impulsada con los descubrimientos de Pasteur sobre la “teoría germinal de las enfermedades infecciosas”: toda enfermedad infecciosa tiene una causa.
Joseph Lister profesor de cirugía en Glasgow, se le considera el padre de la asepsia, al darse cuenta de la relación de los microorganismos de Pasteur con la infección de las heridas, en 1860 empezó a usar el fenol como desinfectante en los quirófanos y en los instrumentos quirúrgicos. La asepsia se hace usual en 1867 cuando Lister publica sus trabajos.
En 1890 Carl Flügge microbiólogo alemán que estudia las enfermedades infecciosas como la tuberculosis y la malaria, sugiere la necesidad de usar máscara, al transmitirse por “gotitas” la infección.

En 1897 Mikulicz-Radecki (1850-1905) cirujano rumano apoya en 1897 el uso de la máscara; junto con Gustav Neuber y Ernst Bergmann fue uno de los tres grandes cirujanos que usaron la asepsia. Entre 1848 y 1914 la cirugía se estaba convirtiendo en una técnica. Viena era una de los centros más importantes, donde destaca Billroth (1829-1894) creador de la cirugía moderna. Mikulicz acaba medicina en 1875 y pasa a ser su asistente, en 1877 pasa a encargarse de una sala del Hospital general de Viena y en 1879 Billroth le envía a Inglaterra para aprender “técnicas antisépticas de Lister”. En 1897 monta en Breslau el quirófano antiséptico más moderno de Europa.
Bibliografía:
National Gegraphic; “Las máscaras durante la peste” 2020
https://historia.nationalgeographic.com.es/a/mascaras-medievales-para-evitar-peste-negra_15176
López-Goñi, Ignacio; “El origen de la peste en Europa: ¿el cambio climático? Investigación y ciencia, 10 de marzo de 2015, SciLogs MEDICINA Y BIOLOGÍA
Haeger, Knut; “Historia de la cirugía”. Madrid, Editorial Raíces, 1993.
file:///C:/Users/Usuario/Downloads/473-Texto%20del%20art%C3%ADculo-1463-1-10-20160426%20(1).pdf
Spooner, John L. “History of Surgical face masks”, The myths, the masks, and the men and women behind them
https://www.sciencedirect.com/sdfe/pdf/download/eid/1-s2.0-S0001209208713590/first-page-pdf
Historia de la Medicina; “Jan Mikulicz-Radecki “
https://www.historiadelamedicina.org/mikulicz.html
“Jan Mikulicz-Radecki (1850-1905): His impact on modern medicine”
Article (PDF Available) in Clinics in Dermatology 30(1):129–136 · February 2012 with 1,138 Reads
DOI: 10.1016/j.clindermatol.2011.05.004
Andrzej Grzybowski, MD, PhDJan Mikulicz-Radecki (1850-1905): His impact on modern medicine Andrzej Grzybowski MDa,b,⁎, Jarosław Sak MDcaDepartment of Ophthalmology, PoznańCity Hospital, ul. Szwajcarska 3, 61-285 Poznań, PolandbMedical Faculty, University of Warmia and Mazury, Olsztyn, PolandcDepartment of Ethics and Human Philosophy, Medical University of Lublin, Szkolna 18, 20-124 Lublin, Polan
Laval R, E; “Apuntes históricos sobre el manejo de la infección en el desarrollo de la cirugía Revista chilena de infectología” Rev. chil. infectol. v.27 n.3 Santiago jun. 2010
CRASSH– Centre for research in the arts, social sciences and humanities. “Cnristos-Lynteris”
http://www.crassh.cam.ac.uk/people/profile/christos-lynteris