
La secuenciación del genoma humano determina la secuencia completa de ADN en el genoma de un organismo (el orden de las bases A, C, G y T en un fragmento de ADN): Secuencia de los cromosomas de un organismo con ADN, el contenido en el de mitocondrias y en las plantas en cloroplastos.
La secuenciación de genes permite a los científicos identificar variantes funcionales de los estudios de asociación y mejorar el conocimiento a disposición de los investigadores interesados en la biología evolutiva, y sentar las bases para predecir susceptibilidad a la enfermedad y la respuesta a los fármacos.
Una de las mayores sorpresas surgidas con la secuenciación del genoma humano es el pequeño número de genes que codifican proteínas, antes se suponía que nuestro genoma incluía 100.000 genes codificadores de proteínas, el número verdadero oscila entre 20.000 y 25.000.
Al alinear los genomas secuenciados, se pueden obtener las mutaciones somáticas producidas, como las sustituciones de bases.
Secuenciación del ADN

Reacción en cadena de la polimerasa (PCR)
Marcado de las moléculas a secuenciar por radiactividad o fluorescencia
Métodos clásicos de secuenciación:
Químico de Maxam y Gilbert
Enzimático de Sanger
Separación de las cadenas de ADN marcadas por electroforesis en geles desnaturalizantes
Segmentación automática empleando el método enzimático:
Segmentación con cebadores fluorescentes
Secuenciación con terminadores fluorescentes
Secuenciación de alto rendimiento o “next-generation”
Se pasa de hacer secuenciación a trozos, a lectura de los genomas de manera completa. Las tecnologías de secuenciación de alto rendimiento son capaces de paralelizar muchas operaciones de secuenciación, produciendo miles o millones a la vez, reduciendo los costos , el coste de cada nucleótido pasó de 10 $ en 1990 a 0.01 $ en 2005.
Son las llamadas también secuenciaciones de nueva generación o “next-generation sequencing” (NGS).

Financiado por instituciones públicas y privadas, así como desarrolladas y comercializadas dentro de la empresa privada por las compañías de biotecnología.
Este tipo de secuenciación a gran escala ha permitido llevar a cabo una lectura eficiente del genoma humano llegando a encontrar incluso regiones no definidas en el genoma de referencia.
Ha producido la identificación de SNPs ( análisis de polimorfismos de una sola base) aún no descritos contribuyendo a un aumento de la tasa de descubrimiento de variantes mediante el estudio de base de un gran número de genomas de diversas poblaciones humanas. De utilidad en la identificación de nuevas variantes, aquellas con relevancia clínica.
Las direcciones futuras para la evolución de NGS incluye su uso para analizar lo llamado “biopsia líquida”, analizando las células tumorales circulantes (CTC) por la sangre, que son células que se desprenden del tumor y viajan a otras partes del cuerpo, su uso es útil tanto en el tratamiento de la enfermedad como en el seguimiento de la evolución, en particular en cánceres de pulmón. No solo se conocerá el estado del tumor en tiempo real sino que, dada su simplicidad, se podrá repetir cuantas veces se quiera para conocer con precisión, la evolución del mismo. Permite determinar el tratamiento adecuado para cada paciente, evitando administrar fármacos o tratamientos que pueden causar efectos molestos secundarios o que no sean realmente efectivos.
Hitos en la secuenciación del ADN
1953; Descrubrimiento de la estructura de la doble hélice de ADN por Watson y Crick.
1972; Tecnología del ADN recombinante, permite el aislamiento de fragmentos definidos de ADN.
1975; Primer genoma secuenciado del bacteriófago X174 por Fred Sanger publicado en Nature, la técnica para leer el ADN consistía en copiar el proceso natural de replicación del ADN.
1977; Se desarrollan métodos de secuenciación:
Allan Maxam y Walter Gilbert, publican “ Secuenciación del ADN mediante degradación químicas”.
Fred Sanger, publica “Secuenciación del ADN mediante síntesis enzimática”.
1980; Fred Sanger y Wally Gilbert reciben el Premio Nobel de química.
1985; Kary Mullis da a conocer la técnica PCR (reacción en cadena e polimerasa) que permite copiar genes específicos con gran rapidez, replicando pequeños fragmentos de ADN.
1986; El laboratorio de Leroy E. Hood en el Instituto de Tecnología de California y Smith anuncian la primera máquina semiautomática de secuenciación de ADN.
1993; Kary Mullis recibe el Premio Nobel de Química.
Bibliografía:
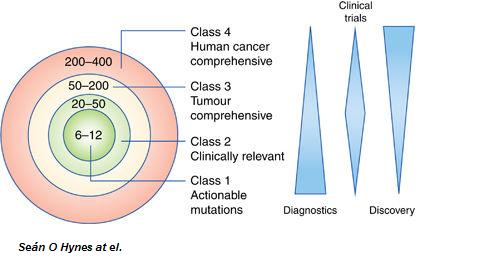
Seán O Hynes, Brendan Pang, Jackeline A James, Perry Maxwell & Manuel Salto-Tellez; “Tissue-based next generation sequencing: application in a universal healthcare system”, British Journal of Cancer 2017
Friedman AA, Letai, Fisher DE, Flaherty KT; “Precisión medicine for cáncer with next-generation diagnostics. Nat Rev Cancer 2015
Souilmi Y, Lancaster AK, Jung JY, Rizzo E, Hawkins JB, Powles R, Amzazi S, Ghazal H, Tonellato PJ, Wall DP; “Scalable and cost-efective NGS genotyping in the cloud. BMC Med Genomics, 2015
Jeremy Mark/ Lubert Stryer/ John L Tymoczko;“Bioquímica”Ed. Reverte, 6ª edición, 2007
Links relacionados:
Parque científico de Madrid, Servicios de Genómica
https://fpcm.es/servicios-cientificos/
Universidad de Córdoba, Servicio de apoyo a la investigación
https://www.uco.es/servicios/scai/genomica.html
Universidad de Navarra, Medicina onco-hematología
http://www.unav.edu/web/vida-universitaria/detalle-opinion2?articleId=13210930
Francisco Martínez-Abarca: Métodos de secuenciación masiva
